 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某恒温密闭容器中,加入1 mol A(g)发生反应A(g)=B()+C(g) ΔH=+ Q kJ·mol-1(Q>0)并达到平衡。缩小容器体积,重新达到平衡,C的浓度比原平衡的浓度大。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗∶n(C)消耗=1∶1
C.保持体积不变,向平衡体系中加入B,平衡不可能向逆反应方向移动
D.若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q kJ
 答案
答案
B、平衡时,单位时间内n(A)消耗∶n(C)消耗=1∶1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“某恒温密闭容器中,加入1 mol A(g)发生反应A(g)=…”相关的问题
更多“某恒温密闭容器中,加入1 mol A(g)发生反应A(g)=…”相关的问题

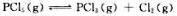 平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数
平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数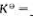 ().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。















