题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某一化学反应,在298 K和大气压力下进行,当反应进度为1 mol时,放热 40.0kJ。若使反应通过可
逆电池来完成,反应进度相同,则吸热4.0kJ。(1)计算反应进度为1mol时的熵变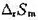 ;(2)当该反应不通过可逆电池完成时,求环境的熵变和隔离系统的总熵变,隔离系统的总熵变值说明了什么问题;(3)计算系统可能做的最大功的值。
;(2)当该反应不通过可逆电池完成时,求环境的熵变和隔离系统的总熵变,隔离系统的总熵变值说明了什么问题;(3)计算系统可能做的最大功的值。
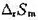 ;(2)当该反应不通过可逆电池完成时,求环境的熵变和隔离系统的总熵变,隔离系统的总熵变值说明了什么问题;(3)计算系统可能做的最大功的值。
;(2)当该反应不通过可逆电池完成时,求环境的熵变和隔离系统的总熵变,隔离系统的总熵变值说明了什么问题;(3)计算系统可能做的最大功的值。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“某一化学反应,在298 K和大气压力下进行,当反应进度为1 …”相关的问题
更多“某一化学反应,在298 K和大气压力下进行,当反应进度为1 …”相关的问题
 ,已知当HI的浓度m=1×10-4mol·kg-1时,E=0.97 V,当m=3.0 mol·kg-1时,E=0.41 V,电极Au+|Au(s)的标准电极电势
,已知当HI的浓度m=1×10-4mol·kg-1时,E=0.97 V,当m=3.0 mol·kg-1时,E=0.41 V,电极Au+|Au(s)的标准电极电势 =1.68 V。试求:(1) HI溶液浓度为3.0 mol·kg-1时的离子平均活度因子γ±;(2) AuI(s)的活度积常数
=1.68 V。试求:(1) HI溶液浓度为3.0 mol·kg-1时的离子平均活度因子γ±;(2) AuI(s)的活度积常数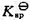 。
。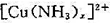 离子中的x值;<2)该配合物离子的迁移数。
离子中的x值;<2)该配合物离子的迁移数。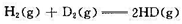
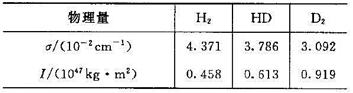
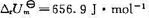 ,HD、H2、D2的有关数据如下:
,HD、H2、D2的有关数据如下: