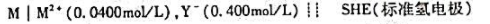题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(
在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(
在一定的温度下,为使电池
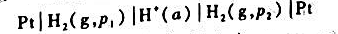
的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(填>,<,=.)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定的温度下,为使电池
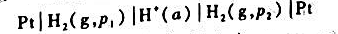
的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(填>,<,=.)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H…”相关的问题
更多“在一定的温度下,为使电池的电动势E为正值,则必须使氢电极中H…”相关的问题
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变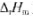 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
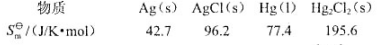 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数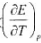
自发电池: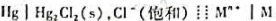 。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
用下列电池按直接电位法测定草酸根离子浓度。
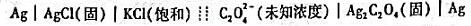
(1)推导出pC2O4与电池电动势之间的关系式
(2)若将一未知浓度的草酸钠溶液置入此电池,在25℃时测得电池电动势为0.402V,Ag-AgCl电极为负极,计算未知溶液的pC2O4。(已知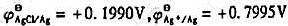 )
)
A.电位的单位与电压、电动势一样,都是伏特
B.电场中某点电位大小等于电场力将单位正电荷从该点移到参考电位点所做的功
C.无论参考电位点选在何处,电源的正极电位总为正值
D.参考电位点的电位值永远为零
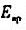 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。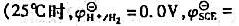
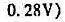
下列电池的电动势为0.460V。计算反应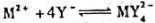 生成的配合物
生成的配合物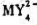 的稳定常数
的稳定常数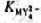 (已知
(已知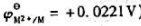 )。
)。