 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知Fe3++e=Fe2+,ϕθ=0.77V,今测得ϕ(Fe3+/Fe2+)=0.73V,则说明电极溶液中的必定是().
A.c(Fe3+)<1mol·L-1
B.c(Fe2+)<1mol·L-1
C.c(Fe3+)/c(Fe2+)>1
D.c(Fe3+)/c(Fe2+)<1
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.c(Fe3+)<1mol·L-1
B.c(Fe2+)<1mol·L-1
C.c(Fe3+)/c(Fe2+)>1
D.c(Fe3+)/c(Fe2+)<1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知Fe3++e=Fe2+,ϕθ=0.77V,今测得ϕ(Fe…”相关的问题
更多“已知Fe3++e=Fe2+,ϕθ=0.77V,今测得ϕ(Fe…”相关的问题
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
重量分析法用于测定矿石中的磁铁矿(Fe3O4)的含量。称取1.5419g试样,用浓盐酸溶解后,得到Fe2+和Fe3+的混合溶液。加入硝酸将Fe2+氧化至Fe3+,稀释后用氨水将Fe3+沉淀为Fe(OH)3。将沉淀过滤,洗涤和灼烧后得0.8525gFe2O3,计算Fe2O3的质量分数?已知摩尔质量:Fe2O3为159.69g·mol-1Fe3O4为231.55g·mol-1.
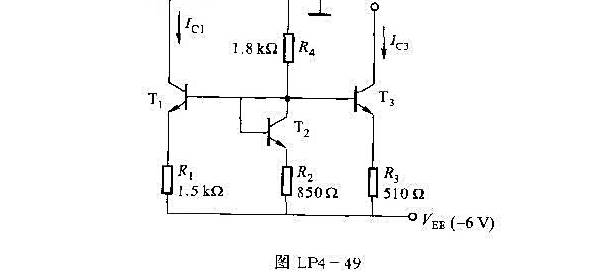
,试求IC1、IC3和T3侧的输出交流电阻Rs3.

A.升高
B.不变
C.降低
D.电势变化与CN-无关
A.氧化性
B.还原性
C.碱性
D.酸性