 更多“温度升高,反应速率加快,说明是吸热反应。()”相关的问题
更多“温度升高,反应速率加快,说明是吸热反应。()”相关的问题
第2题
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算(1)400K时,反应
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
第6题
反应当反应在一定温度下达到化学平衡后,下列说法正确的是().A、升高温度可使化学平衡向正反应
A.升高温度可使化学平衡向正反应方向移动
B.#图片1$#
C.反应物的分压等于生成物的分压
D.加入催化剂,可使化学平衡向正反应方向移动
第7题
使用某些头孢菌素或其他药物期间,饮酒可能引起“双硫仑样”反应,临床常见的表现不包括()。
A.喉头水肿、尿潴留
B.血压升高或降低、心率加快
C.发热、血管扩张、面色潮红
D.头痛、胸闷、气急、出汗
E.兴奋、躁动,后期转为抑制状态
第8题
标准状态下的某化学反应,>0,<0。根据勒夏特列原理,升高温度时平衡右移;但根据公式反应的将增大
标准状态下的某化学反应,>0,<0。根据勒夏特列原理,升高温度时平衡右移;但根据公式反应的将增大
点击查看答案
标准状态下的某化学反应,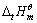 >0,
>0, <0。根据勒夏特列原理,升高温度时平衡右移;但根据公式
<0。根据勒夏特列原理,升高温度时平衡右移;但根据公式

反应的 将增大,不利于反应向右进行。哪一种判断是正确的?
将增大,不利于反应向右进行。哪一种判断是正确的?
第10题
右下表列出HI分解反应(2HI=H2(g)+I2(g))在不同温度下的反应速率,试用两种方法确定该反应的活化能.
右下表列出HI分解反应(2HI=H2(g)+I2(g))在不同温度下的反应速率,试用两种方法确定该反应的活化能.
点击查看答案
第11题
下列有关反应级数和反应分子数的说法中,正确的是()
下列有关反应级数和反应分子数的说法中,正确的是()
点击查看答案
A、反应级数一定是正整数
B、反应分子数可以是正整数或零
D、反应分子数只能是 1、2或3
C、反应级数随温度升高而增大


 如果结果不匹配,请
如果结果不匹配,请 
















