 更多“下列溶液浓度均为0.1mol/L,哪一溶液的凝固点最低()。”相关的问题
更多“下列溶液浓度均为0.1mol/L,哪一溶液的凝固点最低()。”相关的问题
A.NaCN(Ka=6.2x10-10)
B.NaAc(Ka=1.7x10-5)
C.C6H5Na(Ka=1.0x10-10)
D.CH3NH2(Ka=2.3x10-11)
应速率为0.10mol·L-1s-1,计算:(1)速率常数k;(2)当c(H2)=0.60mol·L-1,c(I2)=0.1mol·L-1,c(HI)=0.20mol·L-1时的起始反应速率.
A、NaH2PO4-K2HPO4溶液
B、0.1mol·L-1NaOH与0.2mol·L-1NH4Cl等体积混合溶液
C、0.1mol·L-1HAc与0.1mol·L-1NaOH等体积混合溶液
D、NH4Cl-NH3溶液
【题目描述】
13.下列溶液中微粒的物质的量浓度关系正确的是 A.室温下,向0.01 mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO2-4)>c >c(OH-)=c(H+)
B.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
D.25℃时,pH=4.75、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+C(H+)
| 【我提交的答案】: |
| 【参考答案与解析】: 正确答案:AC |
【我的疑问】(如下,请求专家帮助解答)
D项怎么判断??它们体积不相同啊?
下列情况引起什么误差?若是系统误差,如何减免或消除?
A.蒸馏水中含微量被测离子
C.滴定时溅出溶液
B.滴定管未校正
D.用失去部分结晶水的硼砂为基准物质标定盐酸浓度
E.天平砝码被轻微腐蚀
F.试样未充分混匀
G.称量试样时吸收了水分
H.读数时最后一位数字估计不准
当存在碘催化剂时,氯苯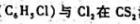 ,溶液中有以下平行二级反应:
,溶液中有以下平行二级反应:
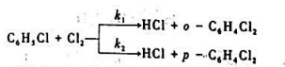
在室温、碘的浓度一定的条件下,当C6H5CI和Cl2在CS2溶液中的初始浓度均为0.5mol.dm-3时,30min后有15%的C6H5CI转化为o-C6H4Cl2有25%的C6H5CI转化为p-C6H4Cl2.试求反应速率常数k1和k2.


 如果结果不匹配,请
如果结果不匹配,请 
















