 更多“用莫尔法测定Cl-时,下列离子中干扰测定的是()。”相关的问题
更多“用莫尔法测定Cl-时,下列离子中干扰测定的是()。”相关的问题
【题目描述】
18.(10分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4===2ClO2↑+Na2SO4+O2↑+2H2O

用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是▲。
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子的含量应不超过0.2mg·L-1。
饮用水中CIO2、CIO2的含量可用连续碘量法进行测定。CIO2被I-还原为CIO-2、Cl-的转化率与溶液pH的关系如右图所示。当pH≤2.0时,CIO-2也能被I-完全还原成Cl-。反应生成的I2用标准Na2S2O3溶液滴定: ①请写出pH≤2.0时,CIO-2与I-反应的离子议程式▲。 ②请完成相应的实验步骤: 步骤1:准确量取V mL水样加入到锥形瓶中。 步骤2:调节水样的pH为7.0~8.0。 步骤3:加入足量的KI晶体。 步骤4:加少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。 步骤5:▲。 ③根据上述分析数据,测得该饮用水样中CIO-2的浓度为▲mol·L-1(用含字母的代数式表示。) ④若饮用水中ClO-2的含量超标,可向其中加入适量的Fe2+将ClO-2还原成Cl-, 该反应的氧化产物是▲(填化学式)。
(1)方法二制备的ClO2中不含Cl2

【题目描述】
7.在下列各溶液中,离子一定能大量共存的是A.强碱性溶液中:K+、、Al3+、Cl-、SO2-4
B.含有0.1 mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO-3
C.含有0.1 mol·L-1Ca2+的溶液中:Na+、K+、CO2-3、Cl-
D.室温下,Ph=1的溶液中:Na+、Fe3+、NO-3、SO2-4
| 【我提交的答案】:C |
| 【参考答案与解析】: 正确答案:D |
答案分析:
【我的疑问】(如下,请求专家帮助解答)
D选项怎么解说,我对离子共存还不太了解
为什么用X射线粉末法测定晶胞参数时常用高角度数据(有时还根据高角度数据外推至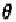 =90°),面测定超细晶粒的结构时要用低角度数据(小角散射)?
=90°),面测定超细晶粒的结构时要用低角度数据(小角散射)?
下列情况引起什么误差?若是系统误差,如何减免或消除?
A.蒸馏水中含微量被测离子
C.滴定时溅出溶液
B.滴定管未校正
D.用失去部分结晶水的硼砂为基准物质标定盐酸浓度
E.天平砝码被轻微腐蚀
F.试样未充分混匀
G.称量试样时吸收了水分
H.读数时最后一位数字估计不准
【题目描述】
某二级公路路基压实施工中,用灌砂法测定压实度,测得灌砂筒内量砂质量为5820g,填满标定罐所需砂的质量为3885g,测定砂锥的质量为615g,标定罐的体积3035cm3。灌砂后称灌砂筒内剩余砂质量为1314g。试坑挖出湿土重为5867g,烘干土重为5036g,室内击实试验得最大干密度为1.68g/cm3,试求该测点压实度和含水率。
【我提交的答案】:
【参考答案分析】:答:砂的密度:
填满试坑砂的质量:mb=m1-m4-m2=5820-1314-615=3891(g);
土体湿密度:

土体含水率:

土体干密度:

压实度:

【我的疑问】(如下,请求专家帮助解答)
土体的干密度的算法好像不对吧,
应该是土的湿密度/1+含水率吧 那个0.1是怎么回事?
A.低价离子的电极易制作,高价离子的电极不易制作
B.能斯特方程对高价离子不适用
C.高价离子的电极还未研制出来
D.测定高价离子的灵敏度低,测量的误差大


 如果结果不匹配,请
如果结果不匹配,请 
















