 更多“反应温度、压力对转化率、产品分布及质量有什么影响?”相关的问题
更多“反应温度、压力对转化率、产品分布及质量有什么影响?”相关的问题
第4题
在770K,100.0kPa下,反应达到平衡,此时NO2</sub>的转化率为56.0%,试计算:(1)该温度下反应的标准平
在770K,100.0kPa下,反应达到平衡,此时NO2</sub>的转化率为56.0%,试计算:(1)该温度下反应的标准平
点击查看答案
在770K,100.0kPa下,反应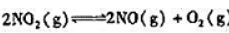 达到平衡,此时NO2的转化率为56.0%,试计算:
达到平衡,此时NO2的转化率为56.0%,试计算:
(1)该温度下反应的标准平衡常数Kθ;
(2)若要使NO2的转化率增加到80.0%,则平衡时压力为多少?
第5题
催化剂的活性是衡量催化剂效能大小的标准,在工业上往往用反应物的转化率表示或用一特定反应达到规定的转化率所需要的反应条件来表示,即达到同样的转化率时,反应温度和压力越低,(),催化剂活性越高。
A.反应器体积越小
B.催化剂装填量越小
C.空速越大
D.空速越小
第6题
温度T时,将PCl5(g)通入一密闭容器中,发生下列反应:平衡时测得容器内的压力为300kPa,PCl5
温度T时,将PCl5(g)通入一密闭容器中,发生下列反应:平衡时测得容器内的压力为300kPa,PCl5
点击查看答案
温度T时,将PCl5(g)通入一密闭容器中,发生下列反应: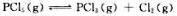 平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数
平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数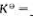 ().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。


 如果结果不匹配,请
如果结果不匹配,请 
















