 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知邻苯二甲酸氢钾(KHP)的摩尔质量201.2g/mol,用它来标定0.1mol/L的NaOH溶液,每次约用NaOH溶液2500mL,应称取KHP质量大约为()
A.0.5g
B.0.25g
C.0.1g
D.0.05g
E.1.0g
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.5g
B.0.25g
C.0.1g
D.0.05g
E.1.0g
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知邻苯二甲酸氢钾(KHP)的摩尔质量201.2g/mol,…”相关的问题
更多“已知邻苯二甲酸氢钾(KHP)的摩尔质量201.2g/mol,…”相关的问题
A.0.4g
B.0.5g
C.0.6g
D.1g
已知邻苯二甲酸(H2C8H4O4)的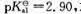 求总浓度为0.050mol·L-1pH为2.50的H2C8H2O4-HC8H4O4缓冲溶液的缓冲容量。
求总浓度为0.050mol·L-1pH为2.50的H2C8H2O4-HC8H4O4缓冲溶液的缓冲容量。
于稀碱溶液中并加热(60℃)使之溶解,冷却后,加入醋酸酸化并移入250mL容量瓶中,加入0.03000mol·L-1Hg
(CIO4)2标准溶液25.00mL,稀释至刻度,放置待下述反应发生:
Hg2++2C12H11N2O3-=Hg(C12H22N2O3)2
过滤弃去沉淀,滤液用干烧杯接收.吸取25.00mL滤液,加入10mL0.01mol·L-1MgY溶液,释放出的Mg2+在pH=10时以铬黑T为指示剂,用0.0100mol·L-1EDTA滴定至终点,消耗3.60mL.计算试样中苯巴比妥钠的质量分数.
写出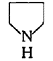 (四氢吡咯)及
(四氢吡咯)及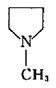 (N-甲基四氢吡咯)分别与列试剂反应的主要产物(如果能发生反应的话)。
(N-甲基四氢吡咯)分别与列试剂反应的主要产物(如果能发生反应的话)。
a.苯甲酰氯
b.乙酸酐
c.过量碘甲烷
d.邻苯二甲酸酐
e.苯磺酰氯
f.丙酰氯
g.亚硝酸
h.稀盐酸
5.51℃,摩尔熔化焓ΔfbhHm(C6H6)=9.832kJ·mol-1.液态水和固态苯的摩尔定压热容分别为Cp,m(H2O,I)=75.37J·mol-1·K-1及Cp,m(C6H6,s)=122.59J·mol-1·K-1.今有两个用绝热层包围的容器,一容器中为0℃的8molH2O(s)与2molH2O(l)呈平衡,另一容器中为5.51℃的5molC6H6(I)与5molC6H6(s)呈平衡.现将两容器接触,去掉两容器间的绝热层,使两容器达到新的平衡态.求过程的ΔS.
(1)求出该化合物的实验式.
(2)推断该化合物的化学式,并利用以上实验事实证明你的推论.