 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在洗涤锥形瓶的操作中,正确的操作为()。
A.先用水或水一洗涤灵洗,若未洗净,再考虑选择其它洗涤剂洗
B.先用铬酸洗液浸泡除去污染物,然后用氢氧化钾—乙醇液除去油污,再用水一洗涤灵洗洗净
C.先用氢氧化钾一乙醇液除去油污,然后用铬酸洗液浸泡除去污染物,最后用水洗净
D.只能用铬酸洗液浸泡,才能将锥形瓶洗净
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.先用水或水一洗涤灵洗,若未洗净,再考虑选择其它洗涤剂洗
B.先用铬酸洗液浸泡除去污染物,然后用氢氧化钾—乙醇液除去油污,再用水一洗涤灵洗洗净
C.先用氢氧化钾一乙醇液除去油污,然后用铬酸洗液浸泡除去污染物,最后用水洗净
D.只能用铬酸洗液浸泡,才能将锥形瓶洗净
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在洗涤锥形瓶的操作中,正确的操作为()。”相关的问题
更多“在洗涤锥形瓶的操作中,正确的操作为()。”相关的问题
用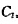 群的元进行相似变换,证明4个对称操作分四类。[提示:选群中任意一个操作为S,逆操作为S-1,对群中某一个元(例如
群的元进行相似变换,证明4个对称操作分四类。[提示:选群中任意一个操作为S,逆操作为S-1,对群中某一个元(例如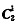 )进行相似变换,若
)进行相似变换,若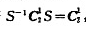 ,则
,则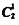 自成一类。]
自成一类。]
A.先用铬酸洗液浸泡除去污染物,然后用氢氧化钾—乙醇液除去油污,再用水一洗涤灵洗洗净
B.由于锥形瓶一般均有刻度,因此可用锥形瓶代替量筒使用
C.将锥形瓶内溶液加热煮沸,最好是在石棉网上冷却半分钟后再用自来水冷却
D.若锥形瓶内残留物不能用瓶刷洗去,只能用瓶刷蘸去污粉,用机械磨擦的原理清洗锥形瓶
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4·7H2O。
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体
Ⅴ.煅烧FeCO3,得到Fe2O3固体
已知:NH4HCO3在热水中分解
问题一、Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是()
问题二、Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用()
问题三、Ⅲ中,生成FeCO3的离子方程式是()。假设FeCO3浊液长时间暴露在空气中,会有部分固体外表变为红褐色,该变化的化学方程式是()
问题四、Ⅳ中,通过检验来判断沉淀是否洗涤干净。检验的操作是()。
问题五、已知煅烧FeCO3的化学方程式是 。现煅烧464.0kg的FeCO3,得到316.8kg产品。假设产品中杂质只有FeO,则该产品中Fe2O3的质量是()kg。(摩尔质量/g·mol-1:FeCO3116Fe2O3160FeO72)
。现煅烧464.0kg的FeCO3,得到316.8kg产品。假设产品中杂质只有FeO,则该产品中Fe2O3的质量是()kg。(摩尔质量/g·mol-1:FeCO3116Fe2O3160FeO72)
A.1、2、3、4
B.1、3
C.3、4
D.1、2、3
A.称取试样1.7g,于250mL锥形瓶中,用50mL蒸馏水溶解
B.加入10滴溴甲酚绿-甲基红指示剂
C.滴定至溶液刚刚变色时,煮沸2min,冷却后继续滴定至暗红色为终点
D.做空白试验
E.做对照试验
A.在信贷系统中取消放款通知书号,然后删除放款业务即可
B.在信贷系统中直接撤销小额贷款卡放款业务即可
C.在综合业务系统“预放款”交易中撤销
D.在综合业务系统“放款”交易中撤销
A.滴定时,不用排出滴定管下口的气泡
B.滴定时需加入其他指示剂
C.锥形瓶用蒸馏水洗净后,直接移取一定体积的未知浓度的H2O2溶液
D.酸式滴定管用蒸馏水洗净后,直接加入已知浓度的KMnO4溶液